2023年7月13日,Nature communications在线发表了一篇题为“Structural journey of an insecticidal protein against western corn rootworm"的研究论文。作者鉴定了一种对 WCR 有活性的杀虫蛋白 Mpf2Ba1,并对非 Bt 生物体的 PFP 进行了全面的结构功能表征,揭示了孔形成的关键分子机制。

成孔蛋白 (PFP) 是一类主要的可溶性蛋白,它们寡聚成环并发生巨大的不可逆构象变化,成为跨膜组装体并突破靶细胞膜。由此产生的孔隙中不受控制的离子流入/流出会造成严重的渗透失衡和毒性,最终导致细胞死亡。
苏云金芽孢杆菌(Bt) 的 PFP 一直是转基因抗虫作物的基础,近三十年被全球种植者使用。PFP提供的抗虫性十分有效,并且具有环境和经济效益。影响北美和欧洲玉米生产并导致重大产量损失的特别具有破坏性的害虫之一是鞘翅目的西部玉米根虫(WCR;Diabrotica virgifera virgifera)。自21世纪初以来,表达Cry3类Bt蛋白(mCry3Aa、Cry3Bb1和eCry3.1Ab)的转基因玉米作物使得这种害虫在北美得到了有效控制。然而,由于WCR在田间种群中产生抗性,这些蛋白遇到了药效降低的情况。由于有用的Bt衍生杀虫蛋白的发现愈加困难,当务之急是从非Bt生物中寻找具有高活性和新作用模式/位点的新型蛋白。
Nature communications发表的那篇文章,作者首先通过WCR 幼虫的人工饲料生物活性筛选,并通过多步纯化过程从蒙氏假单胞菌中分离得到Mpf2Ba1。Mpf2Ba1 是一种 53.2 kDa 的蛋白质,表现出对WCR较好的杀虫效果。紧接着作者解析了 Mpf2Ba1 X 射线结构,并展示了 N 末端残基如何抑制可溶形式单体的缔合。
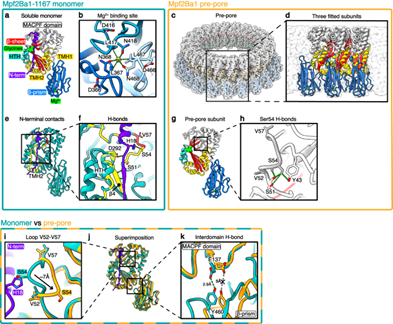
然后,作者证明了肠液存在下的蛋白水解作用会激活单体自组装成前孔,并通过冷冻电镜以 3.1 ? 分辨率重建了前孔。单体和前孔亚基之间微妙但显著的变化揭示了与靶标识别和激活/寡聚化相关的分子机制。热诱导的前孔向孔的转变使我们能够以 2.6 ? 分辨率解析 21 聚体孔冷冻电镜结构,显示孔亚基的显着构象变化及其 HTH 介导的亚基间稳定性。

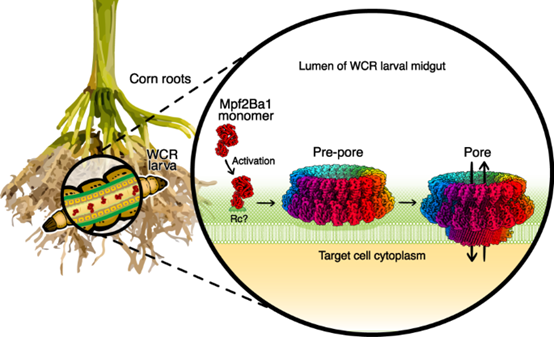
综上,作者鉴定并表征了非 Bt 杀虫蛋白 Mpf2Ba1,并解析了其如何通过在中肠膜上形成孔来有效杀死毁灭性玉米害虫 WCR 的分子机制,该孔的结合位点与目前商业转基因玉米杂交种中使用的杀虫蛋白不同。以受 Mpf2Ba1 保护的玉米为食的 WCR 幼虫摄入由植物根组织表达的 Mpf2Ba1 单体。可溶性单体到达幼虫中肠,并在与靶细胞上尚未识别的受体 (Rc) 结合之前/同时被肠道蛋白酶激活,并寡聚成前孔。前孔转变为不可逆的跨膜孔,使离子流不受控制地穿过质膜,破坏细胞功能并导致幼虫饿死。